金属の銅やマグネシウムを空気中で燃やし、その後重さがどうなるのかを学習します。
「燃えた後の金属の重さ」応用問題
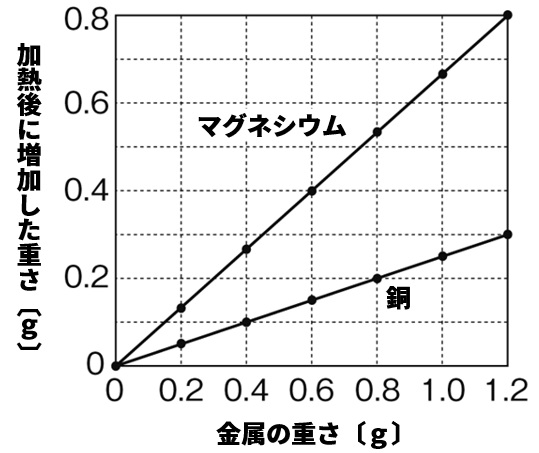 Q:右のグラフは、金属を空気中で完全に燃やしたときの重さの変化を表したものである。これについて、以下の各問いに答えよ。
Q:右のグラフは、金属を空気中で完全に燃やしたときの重さの変化を表したものである。これについて、以下の各問いに答えよ。
(1)金属を空気中で加熱すると、重さが増加するのはなぜか。
(2)右のグラフから、銅と酸素は、重さの比で何:何で反応するとわかるか。
(3)マグネシウム3.0gを空気中で完全に反応させると、加熱後の重さは何gになるか。
(4)銅3.2gを加熱したところ、加熱後の重さが3.8gになった。まだ反応していない銅は何gあるか。
燃えた後の金属の重さ
鉄や銅、マグネシウムのような金属を粉状にして加熱すると、炎を出さずに光や熱を出しながら空気中の酸素と結びつきます。
- 鉄 + 酸素 → 酸化鉄(黒色)
- 銅 + 酸素 → 酸化銅(黒色)
- マグネシウム + 酸素 → 酸化マグネシウム(白色)
このとき、燃やす前の金属の重さと、燃えたあとに増加した重さには次のような関係がみられます。空気中の酸素が結びついた分だけ重さが重くなることがわかります。
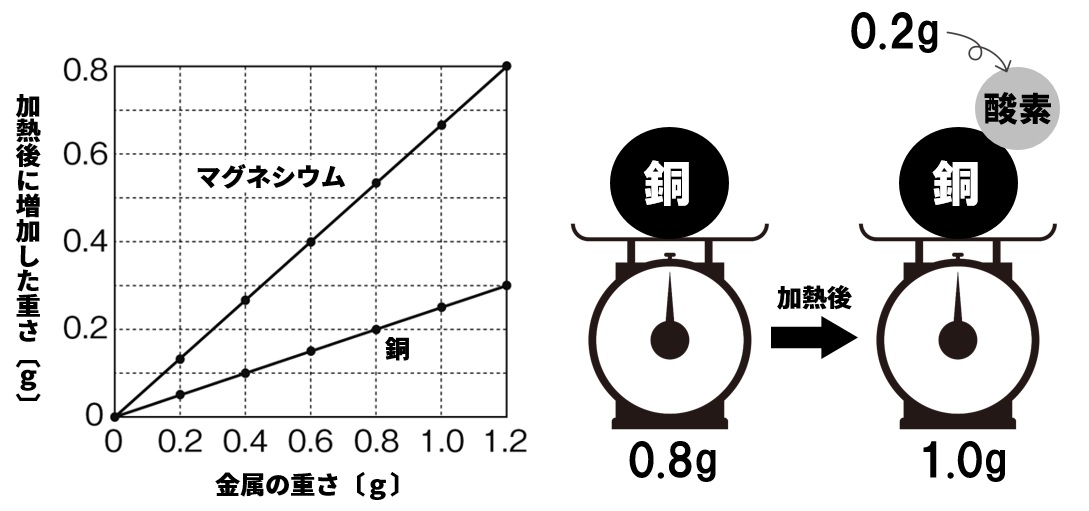
例えば、銅0.8gを空気中で完全に加熱すると、重さが0.2g増加し、加熱後の重さが1.0gになることがわかります。0.8gの銅には酸素が0.2g結びつき、酸化銅が1.0gできるとわかります。
グラフのようすを確認してください。比例のグラフになっていますよね。これは、金属の重さと結びつく酸素の重さの比が決まっていることを表しています。その比は、金属の種類によって異なっていることもわかります。
●金属と結びつく酸素の重さの比
- 銅:酸素=4:1
- マグネシウム:酸素=3:2
この性質を利用すると、加熱後にできる物質の重さを計算で求めることができるようになります。
比を使った計算の方法
例えば、「1.6gの銅を加熱したときに、何gの酸素が結びつくか?」という問題があったとします。
銅と酸素は、重さの比で4:1で反応するので、比を使って次のように計算できます。
4:1=1.6:□
比の左側が4から1.6になっているので、1.6÷4=0.4倍になっています。
比の右側も0.4倍にならないといけないので、1✕0.4=0.4gと計算できます。
このように、反応する比がわかれば、簡単に重さを求めることができるようになります。
「燃えた後の金属の重さ」応用問題 解答
A
(1)空気中の酸素が金属と結びつくから。
結びついた酸素の重さ分だけ重くなります。
(2)4:1
グラフから、0.4gの銅に0.1gの酸素が結びついていることがわかります。簡単な整数比にすると4:1になります。
(3)5g
グラフから、マグネシウムと酸素は重さの比3:2で反応することがわかります。ということは、マグネシウムと酸化マグネシウムの重さの比は3:(3+2)=3:5になることもわかります。
(4)0.8g
次のステップで計算しましょう。
➀結びついた酸素の重さを計算する。
重さが増加した分だけ酸素が結びついているので、3.8ー3.2=0.6g酸素が結びついた。
➁結びついた酸素から反応した銅の重さを計算する。
銅と酸素は重さの比4:1で反応するから、4:1=□:0.6
比の右側が1から0.6になっているので、0.6÷1=0.6倍
比の左側も0.6倍にすると、4✕0.6=2.4gの銅が反応した。
③未反応の銅の重さを計算する。
もともとあった銅の重さから反応した銅の重さを引くと、
3.2ー2.4=0.8g
このように計算します。


コメント