もののあたたまり方の応用問題に挑戦しましょう。今回は、熱量の計算を使う問題になっています。
「水と氷の温度変化」応用問題
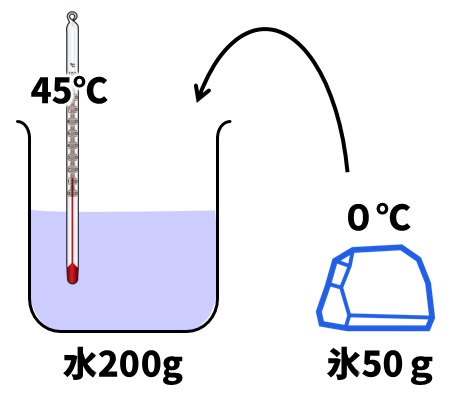
Q:下の図のように、0℃の氷50gと45℃の水200gをまぜ合わせると、何℃の水になるか。ただし、80gの水を1℃上げる熱で、0℃の氷1gを0℃の水1gに変えることができるものとし、熱は容器に吸収されたり、容器の外に逃げたりしないものとする。
熱量の計算方法
今回の問題を解くには、熱量の計算を知っていた方が楽なので、熱量の計算方法をまずはマスターしましょう。
●熱量の計算方法
熱量〔cal〕=水の重さ〔g〕✕温度変化〔℃〕
熱量の単位は〔cal〕と書いてカロリーといいます。1calは1gの水の温度を1℃上げる熱量になります。ということは、水の重さや温度変化とcalは次のような関係になります。
温度変化と熱量
- 水1gを1℃上昇させる → 1cal
- 水1gを2℃上昇させる → 2cal
- 水1gを3℃上昇させる → 3cal
水の重さと熱量
- 水1gを1℃上昇させる → 1cal
- 水2gを1℃上昇させる → 2cal
- 水3gを1℃上昇させる → 3cal
水の重さと温度変化と熱量
- 水1gを1℃上昇させる → 1cal
- 水2gを3℃上昇させる → 6cal
- 水100gを4℃上昇させる → 400cal
水の重さと温度変化を掛け算すれば、熱量calを求めることができますね。
また、1gのものの温度を1℃上げるのに必要な熱量は、ものの状態や物質の種類によって異なります。水と氷であたたまり方が違うのですね。
「水と氷の温度変化」応用問題 解答
まずは、「80gの水を1℃上げる熱で、0℃の氷1gを0℃の水1gに変えることができる」と書いてあるので、熱量の計算をします。
80gの水を1℃上げる熱量は、80g✕1℃=80cal
この80calの熱で、0℃の氷1gを0℃の水1gに変えることができるので、0℃の氷50gを0℃の水50gに変えるには、氷の量が50倍になっているので次の熱量が必要です。
80cal✕50=4000cal
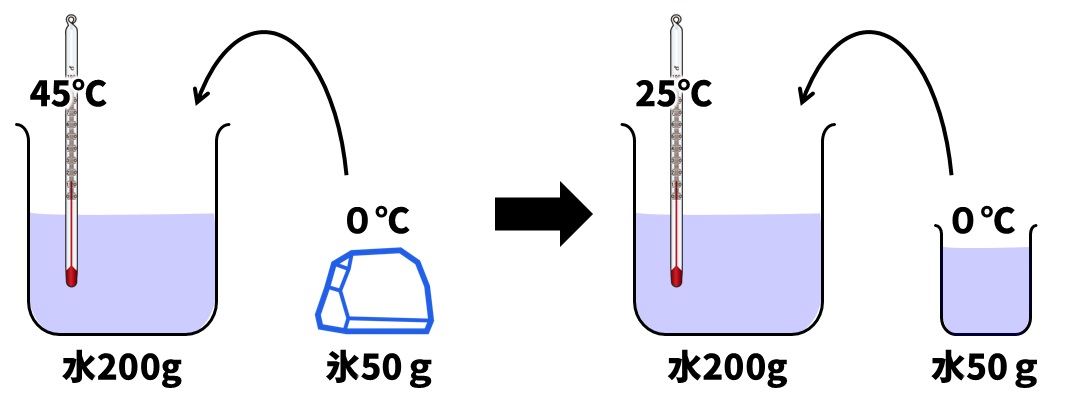
4000calの熱をもらって、0℃の氷50gが解けて0℃の水50gになったということは、混ぜ合わせた45℃の水200gは、4000calの熱を失ったということになります。45℃の水200gは何℃温度が下がるか求めます。
200g✕□=4000cal □=20℃
45℃の水200gは、20℃温度が下がるので25℃の水になります。いったん下の図のように考え、それから25℃の水200gと0℃の水50gを混ぜ合わせ、何℃になるか求めましょう。
てんびん法で解くと次のようになります。
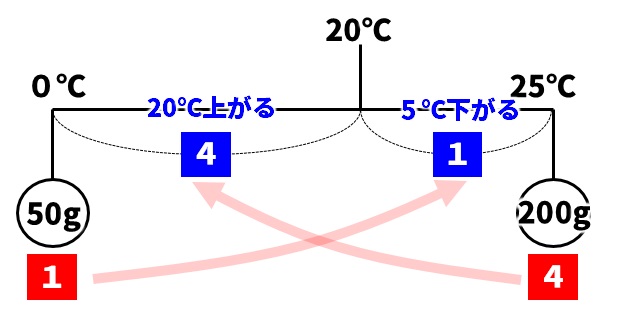
A:20℃
コメント